ELEKTROENSEFALOGRAFİ
Yazanlar:
Betül Baykan, Ebru Altındağ, Ayşe Deniz Elmalı
Son
güncelleştirme tarihi: 19.01.2019
Elektroensefalografi (EEG) beynin
spontan elektriksel aktivitesinin elektrodlar
aracılığı ile kaydedildiği noninvazif inceleme
yöntemidir. Bu inceleme beynin yapısal özelliklerinden çok o anki fonksiyonel
durumunu yansıtır. Bu nedenle yapısal görüntüleme yöntemlerindeki (BT, MRG
gibi) gelişmelere rağmen halen önemini korumaktadır. Özellikle yapısal inceleme
yöntemlerine yansıyan bir patolojik bulgunun olmadığı klinik tablolarda EEG’nin
önemi daha da artar.
EEG, epilepsi
tanısının konulmasında, kesin epilepsi tanısı almış hastaların sınıflaması,
uygun tedavi seçimi ve prognozun belirlenmesinde
ve hastalığın seyrinin takibinde kullanılan en değerli inceleme yöntemidir.
Sadece mental durum bozukluğu ile karakterize nonkonvülzif
status epileptikus (NKSE) tablosunun tanısı için
tanı koydurucu tek inceleme yöntemi iken yavaş virüs hastalıkları, herpes
simpleks ensefaliti ve hepatik ensefalopati gibi bazı özel tabloların tanısı ve takibinde
de çok önemli ipuçları sağlar. Ayrıca uyku ve bozuklukları ile beyin ölümünün
değerlendirilmesinde de EEG kullanılır.

Hans
Berger (1873-1941):
Jena Üniversitesi’nde Otto
Binswanger’in ardından direktör olan bir Alman
nöropsikiyatristidir. Elektroensefalografiyi
1924 yılında ilk kez kaydeden bilim insanı olarak tarihe geçmiştir. Berger’in
beyindeki elektrik aktivitesi konusundaki ilk yayını “Über das Elektrenkephalogramm des
Menschen” 1929 yılında “Archiv
für Psychiatrie und Nervenkrankheiten”
dergisinde yayınlanmıştır ve izleyen 23 yayını ile alfa ve beta aktivitelerini,
çeşitli durumlara bağlı EEG değişimleri tanımlayan kişidir. Uluslararası tanınırlığı
ancak 1935’lerde gerçekleşirken üzücü olan kendi ülkesinde Nazi’ler nedeniyle
bu önemli buluşuna rağmen saygı görmemesidir. Ne yazık ki 1938 yılında emekli
olmasının ardından ilerleyen bir depresyon sonucunda 1941 yılında suisid nedeniyle hayatını kaybetmiştir.
EEG Aktivitesinin
Hücresel Temeli
Beynin elektriksel
aktivitesi hücresel düzeyde biyokimyasal işlemlerden köken alan iyonik akımların
sonucudur. Merkezi sinir sisteminde (MSS) nöronlar ve glial hücreler olmak üzere iki ana hücre tipi bulunur.
Pek çok dendrit ve aksondan oluşan nöronlar üzerlerindeki
sayısız sinaps ile birbirleri ile bağlantı halindedir.
İki lipid tabakalı nöronal hücre membranı hücreyi
hücre dışı ve hücre içi olarak iki alana ayırır. Sodyum ve klor iyonları
hücre dışında yüksek konsantrasyonda iken potasyum
iyonları, negatif yüklü büyük moleküller ve anyonlar hücre içinde yüksek
orandadır. Membranın iki tarafındaki iyon konsantrasyon farklılığı istirahat membran potansiyelini
oluşturur. Hücre içine pozitif yüklü iyonların akışı olarak tanımlanan depolarizasyon membran potansiyelinin daha az negatif
hale gelmesine neden olurken, hücre içine negatif iyonların geçmesi membran
potansiyelini daha negatif hale getirir ve buna da hiperpolarizasyon
denir. Hücrenin tekrar istirahat membran potansiyeline varması Na-K-ATPaz pompası ile olur. Na önemli miktarda hücre içine
girdiğinde membran potansiyeli eşik değere ulaşır, Na kanallarının açılması
ile daha fazla Na girişi aksiyon potansiyelinin yükselen fazını oluşturur.
K iyonunun dışarı çıkması, Na iyonunun içeri girmesinin azalması repolarizasyona neden olarak aksiyon potansiyelinin
düşme fazını oluşturur.
EEG dalgalarının
kaynağını korteksin 3, 5 ve 6. tabakalarında vertikal yerleşim gösteren piramidal
hücrelerin senkronize bir şekilde aktive olması ile ortaya çıkan inhibitör
(IPSP) veya eksitatör (EPSP) özellikte postsinaptik
potansiyeller oluşturur. Bu kayıt için ortalama 6 cm2’lik kortikal
alanın senkron olarak aktive edilmesi gerekmektedir.
Aksiyon potansiyelleri ve glial aktivite ise
EEG’ye minimal katkıda bulunurlar.
İnsan EEG’si
istirahat ve uyanıklık halinde ritmik bir aktivite gösterir. Korteksin spontan
ritimler oluşturan nöron ağlarına sahip olduğu bilinir. Talamo-kortikal bağlantılar yoluyla retiküler ağ ve talamik
nukleuslar kortikal
potansiyelleri uyarır ya da desenkronize eder.
EEG’deki epileptiform aktivite ise epileptojenik odak içindeki nöronlar tarafından senkronize
edilen bir grup hücrenin membran potansiyellerinin paroksismal
depolarizasyon kaymaları sonucu oluşur. Paroksismal
depolarizasyon kayması, bir nöbet öncesi olayıdır
ve sonucunda çok hızlı ve çok fazla sayıda aksiyon potansiyeli oluşturur.
Hücre içi depolarizasyondan kaynaklanan akım
apikal dendrite doğru
yönlenir, tüm nöronun somatodendiritik bölgesini
kapsar ve hücre dışında yüzeyel diken-dalga aktivitesini oluşturur. Paroksismal
depolarizasyon kaymasının ardından oluşan uzamış
hiperpolarizasyon ile iç tepkiler, o nörondan
diğerine yayılır ve hipersenkronizasyon ortaya
çıkar. Ancak anormal ritimlerin fizyolojik temeli ve nöbet aktivitesinin altında
yatan hipersenkronizasyondan sorumlu mekanizmalar
halen iyi açıklanmış durumda değildir.
EEG’nin Kaydedilmesi
EEG’nin kaynağını
oluşturan postsinaptik potansiyeller kortekste
toplanır ve beyni saran yapılardan saçlı deriye yayılarak, saçlı deriden
metal elektrodlar ile kaydedilir. İletken bir
madde ile kaplı her bir elektrodun yeri nazion, inion, sağ ve
sol preauriküler noktalardan yapılan standart
ölçümlerle belirlenir ve Uluslararası 10–20 sistemine göre yerleştirilir.
Her bir elektroddan alınan kayıt montaj
adı verilen bağlantılarla değerlendirilir (Şekil 1). Eski tip EEG
aletlerinde elektrodlar arasındaki potansiyel
farklılıkları amplifikatörlerle yükseltilerek hareket eden kağıt üzerinde yazdırılır, kayıt parametreleri ve montajlar
sonradan değiştirilemezken, günümüzdeki dijital EEG cihazlarında kayıtlar
monitörden izlenebilmekte, kayıt yapılan montajdan sonra diğer montajlara
geçilebilmekte, amplitüd ve diğer parametrelerin her olgu için ve her bulgu
için yeniden ayarlanması mümkün olabilmektedir.
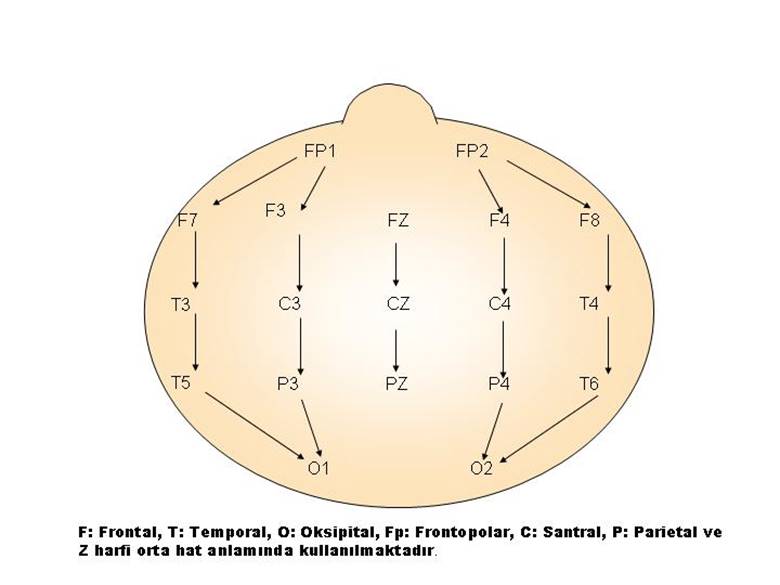
Şekil 1. Standart olarak
kullanılan elektrodların Uluslararası 10-20 sistemine
göre yerleşimleri ve “double banana” olarak da
isimlendirilen longitudinal bipolar montaj oklarla şematik olarak gösterilmiştir.
Aynı elektrodlar mutlaka transvers bir montaj
ile ve unipolar olarak da (örneğin CZ veya şekilde
bulunmayan kulak elektrodlarına bağlayarak) değerlendirilmelidir.
Filtreler EEG’den
gelen görece yüksek ve düşük frekanslardaki dalgaları dışlamak için kullanılır.
EEG cihazının yavaş dalgaların amplitüdünü azaltan
alçak frekans filtresi, hızlı dalgaların amplitüdünü
azaltan yüksek frekans filtresi ve en yaygın elektrik artefaktı olan 50-60 Hz dalgaların amplitüdünü azaltan 50-60 Hz (notch) filtresi olmak üzere 3 çeşit filtresi vardır.
EEG filtrelerinin doğru ayarlanmış olması çok önemlidir, tercih edilen yüksek
frekans filtresi 70 Hz, düşük frekans filtresi 0,5 Hz olmalıdır.
Artefaktlar beyin kaynaklı
olmayan sinyallerdir. Elektrod ve kayıt aletlerinden
kaynaklanan biyoelektriksel olmayan artefaktlar olabileceği gibi beyin kaynaklı olmayan
oküler, kardiyak, glossokinetik, yutkunma, kas
ve hareket artefaktları gibi hastadan kaynaklanan
artefaktlar da biyoelektrik artefaktlardır. Artefaktların
çoğu elektrod ve saçlı deri arasındaki temas bozukluğundan
kaynaklanır. Elektrodun yerinden çıkması, amplifikatörden
kaynaklanan aşırı gürültü, dış kaynaklardan gelen akımlara bağlı artefaktlar, elektrostatik potansiyeller veya intravenöz
infüzyonlara bağlı çeşitli artefaktlar olabilir (Şekil 2). Artefaktların patolojik olarak yorumlanması hasta
için olumsuz sonuçlara yol açabilir.

Şekil 2. Okla işaretli
olan frontal bölgelere sınırlı göz kapatmaya bağlı bulgu delta dalgaları
ile karıştırılmamalıdır.
EEG kaydı genellikle
sessiz, rahat şartlarda, rutin bir EEG için yaklaşık 30 dakika süre ile yapılır.
Öncesinde elektrodların yerleşimi çok önemli
bir hazırlık aşamasıdır. Elektrodlar uygun maddelerle
yapıştırılarak ya da şapka şeklinde kauçuk bantlarla sıkıştırılarak yerleştirilir
ve bazı özel pastalar ya da tuzlu su ile iletkenlikleri sağlanır. EEG çekimi
öncesinde hastanın saçlarının temiz olması önem taşır. Ayrıca açlıkta bazı
değişiklikler görülebileceğinden çekim sırasında hasta tok olmalıdır. EEG
çekimi süresince hasta sakin bir şekilde oturmalı veya uzanmalı ve EEG teknisyeninin
direktiflerine göre gözlerini kapatıp açmalıdır.
Her rutin EEG
çekiminde hiperventilasyon (HV) uygulanır. Burada
amaç bir epileptik odağı aktif hale geçirmektir. Bazı medikal nedenlerle
HV uygulanamadığı durumlar olabilir. Bunlar yakın zamanda geçirilmiş serebrovasküler hastalık, ciddi kardiyopulmoner hastalık, orak hücreli anemi olarak
özetlenebilir. Hastanın şuurunun kapalı olması ve koopere
olmaması gibi nedenlerle de HV uygulanamayabilir. HV süresi minimum 3 dakikadır
ve tercihen 5 dakika uygulanmalıdır. HV ile absans
nöbetlerinin tetiklenmesi ya da jeneralize diken
dalga paroksizmlerinin belirmesi çok tipiktir
(Şekil 3). 16 yaş altında görülen ve jeneralize yavaş dalgalarla ile
karakterize olan HV reaksiyonu iyi bilinmesi gereken bir tablodur. Fizyolojik
olan bu reaksiyonun patolojik olarak rapor edilmesi hasta açısından kötü
olabilecek sonuçlara yol açar. Ayrıca fokal yavaş dalga ve fokal epileptiform aktivite de HV ile aktive olabilir. HV
yaptırılmadığında diagnostik olabilecek çok önemli
bilgiler kaybedilmiş olur. Ayrıca HV sırasında hipokalsemi
ve hipoglisemi gibi metabolik problemlerin de aktive olabileceği ve bu durumun
EEG’yi bozabileceği akılda tutulmalıdır.

Şekil 3. Hiperventilasyon ile tetiklenmiş
olan, hastada klinik olarak dalma nöbetinin eşlik ettiği, 12 saniye süren,
3 Hz jeneralize diken dalga deşarjları görülmektedir.
Aralıklı ışık
uyarımı (intermittent photic stimulation, IFS) da benzer şekilde her rutin EEG’de
mutlaka uygulanması gereken önemli bir aktivasyon yöntemidir. Bazı olgularda
tüm EEG normalken yalnızca IFS’de epileptik aktivite
görülebilir (Şekil 4). Hatta bazen miyoklonik
nöbetler ve daha nadiren diğer nöbet tipleri (absans,
oksipital fokal nöbet veya jeneralize tonik-klonik
nöbet) ortaya çıkabilir. Tümüyle asemptomatik olgularda da IFS’de duyarlılık bulunabileceği unutulmamalıdır.
IFS, HV’den en az 3 dakika sonra başlamalı ve
HV etkisi ile örtüşmesi engellenmelidir. Nasion
noktasının fotik stimülatöre
uzaklığı

Şekil 4. Aralıklı ışık
uyarımı esnasında (photic 15 olarak işaretli)
jeneralize tipte epileptiform
aktivite öncesinde rutin çekim tamamen normalken, 15 Hz ile stimülasyon sırasında
ortaya çıkmış ve tanı açısından değerli bir ipucu oluşturmuştur.
EEG’nin Değerlendirilmesi
EEG bulgularının
değerlendirilebilmesi için öncelikle normal EEG özelliklerinin çok iyi bilinmesi
gereklidir. Her EEG çekiminde önce temel aktivite değerlendirilir. Normal
temel aktivite yaşla, uyanıklık durumuyla, açlık gibi bazı fizyolojik durumlarla
çok belirgin farklılıklar gösterir. Üç aylık bir bebek için normal sayılan
aktivite 3 yaşında bir çocuk için patolojiktir. Benzer şekilde derin uykuda
olan bir erişkinin EEG aktivitesi aynı kişi uyanıkken görüldüğünde ciddi bir
patolojik bulgu anlamına gelebilir.
EEG’de beynin
hemisferleri arasında simetri vardır, bu nedenle
iki yarıkürenin kıyaslanması önemlidir. EEG çekimi sırasında hastanın kullandığı
ilaçlar ve varsa metabolik problemleri mutlaka kaydedilmelidir. Çünkü bazı
ilaçların ve metabolik durumların EEG üzerinde etkileri belirgindir. Ayrıca
epileptik hastanın nöbeti ile EEG çekimi arasındaki süre, yani EEG’nin postiktal mi yoksa interiktal
dönemde mi yapıldığı bazı bulguların yorumu açısından önem taşır.
EEG sonucunda
yorum yaparken görülen bulguları tanımlamayı yeğlemek ve EEG bulgusu ile
klinik tanı arasında yanlış olabilecek bir yakıştırma yapmamak gerekir. EEG
değerlendirmesini mümkünse bu konuda deneyimli uzmanların yani klinik nörofizyologların yapması, ancak her hekimin sonuçları
yorumlayabilmesi gereklidir.
Başlıca
EEG Bulguları
EEG çeşitli frekanslarda
ve amplitüdlerde potansiyeller gösterir (Şekil
5). Temel aktivite yaşa göre değişmekle birlikte normal bir erişkinde
uyanık ve gözler kapalıyken pariyeto-oksipital
bölgelerde 8-12 Hz frekansında bir aktivite görülür, bu aktivite alfa aktivitesi
olarak isimlendirilir. Alfa aktivitesi gözler açılınca kaybolur ya da baskılanır.
Beta aktivitesi 13-25 Hz frekansında frontal ve santral bölgelerde
belirgin olan bir ritimdir. Yüksek amplitüdlü beta aktivitesi genellikle
sedatif-hipnotik bir ilacın kullanıldığını düşündürür.

Şekil 5. Bazı EEG dalgalarının
frekansları görülmektedir.
Normal uyku sırasında EEG’de
farklı dönemler izlenir. Birinci dönem uyku-uyanıklık arası geçiş dönemidir,
alfa ritmi kaybolurken yerini düşük voltajlı yavaş aktivitelere bırakır,
ardından verteks bölgesinde yüksek amplitüdlü
keskin dalgalar belirir. Deneyimsiz bir göz uyanıklık sırasında oluştuğunu
sanarak bu dönemi patolojik olarak yorumlayabilir. İkinci dönemin işareti
frontosantral yerleşimli 12–14 Hz sinüzoidal
yapıdaki uyku iğleridir (Şekil 6). Üçüncü ve dördüncü dönemler yavaş
dalgalı uyku olarak anılır, yüksek amplitüdlü, yaygın ve düzensiz yavaş dalgalardan
oluşur. REM (rapid eye
movement) dönemi ise düşük voltajlı, değişken
frekanslı bir aktivitedir; rüyaların görüldüğü ve hızlı göz hareketlerinin
ve kaslarda atoninin kaydedildiği dönemdir. REM
uyku başlangıcından sonra yaklaşık 90 dakika sonra belirdiği için gündüz
yapılan kısa süreli uyku incelemelerinde genellikle görülmez.

Şekil 6. Fronto-santral bölgelerde
uyku iğleri (ok) ve jeneralize K kompleksi görülmektedir.
EEG’de rastlanabilecek
patolojik bulgular nonspesifik yavaş dalgalar
ve epileptiform aktivite olarak iki ana gruba
ayrılır. Yavaş dalga aktivitesi teta (4-7Hz)
ve delta (1-3Hz) olarak gruplanır. Görülen yavaş dalganın lokalizasyonu önemlidir.
Sıklığı, amplitüdü, varsa ilişkili olduğu diğer
faktörler kaydedilir (Şekil 7). Fokal yavaş dalga bulgusu, %70 olasılıkla
kaydedildiği bölgede yapısal bir beyin lezyonunun varlığını düşündürür. Ancak
bazen bu bulgu lezyonel olmayan fokal bir epilepside
de görülebilmektedir. Fokal voltaj azalması benzer şekilde ilgili gri maddede
lezyon düşündürdüğü gibi subdural ve epidural birikimlerde de rastlanan bir bulgudur.

Şekil 7. Hiperventilasyon (HV) sırasında
normal bir aktivite olan alfa dalgalarının yerini teta,
hatta delta dalgalarına bırakması 16 yaşına dek normal kabul edilmekteyken
erişkin bir hastada patolojiktir.
Yer kaplayıcı
lezyonların incelemesinde EEG bugün önemini kaybetmiş ve yerini yapısal görüntüleme
yöntemlerine bırakmıştır. Ancak kimi zaman yer kaplayan lezyonun epileptojenik potansiyelini araştırmak amacıyla EEG’ye
başvurmak gerekmektedir. Benzer şekilde serebrovasküler hastalıklarda da
EEG önemini kaybetmiştir. Geçici iskemik ataklarda yarıya yakın olguda fokal
yavaşlama görülür. Belirgin bir akut defisiti olan, ancak EEG’si tamamen
normal bulunan bir hastada laküner inme olasılığı
yüksektir. Migrenli ve diğer primer başağrılı
olgularda EEG yapılmasına, ek bir sorun olmadıkça gerek yoktur. Handle denen özel bir tabloda (geçici nörolojik
defisitler ve BOSta lenfositozla
giden başağrılı tablo) EEG’de yavaş dalga aktivitesi
tipiktir.
Dejeneratif beyin
hastalıklarında beyin fonksiyonunu incelemek, epilepsi varlığını araştırmak
ve izlemek amacıyla EEG’ye başvurulur. Alzheimer hastalığında başlangıçta
EEG normalken demansın ileri dönemlerinde, genellikle
3 yıl içinde alfa aktivitesi yerini yaygın teta
aktivitesine bırakır. Huntington hastalığı gibi
bazı tablolarda jeneralize voltaj azalması kaydedilir. Creutzfeldt-Jacob hastalığında tipik EEG bulgusu
varsa tanı açısından patognomoniktir (Şekil
8). Ancak bu EEG bulgusu ileri evrelerde kaybolabilir ve yerini yaygın
ağır bir yavaşlamaya bırakabilir. Benzer şekilde subakut sklerozan panensefalit
(SSPE) (Şekil 9) tablosunda da EEG patognomonik
bulgular verir. Burada ana özellik yavaş dalgalar ve eklenen keskin elemanlardan
oluşan jeneralize deşarjın periyodik aralarla çekim süresince tekrarlamasıdır.
SSPE yurdumuzda hala görülmeye devam ettiğinden bu tip paroksizmlerle karşılaşıldığında periyodik özellik
olup olmadığı araştırılmalıdır.

Şekil 8.
Creutzfeldt-Jacob hastalığı tanısında patognomonik değer taşıyan tipik jeneralize 1 Hz periyodik
keskin dalga kompleksleri izlenmektedir.
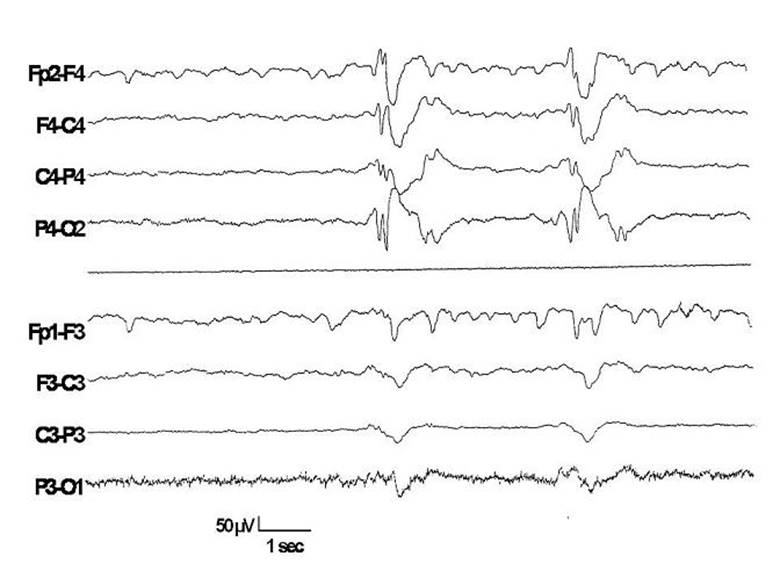
Şekil 9. BOS’da kızamık antikorlarının varlığı ile kanıtlanmış
SSPE tanısı alan bir hastada tanıya götürücü rol oynayan ve patognomonik özellik taşıyan periyodik yavaş dalga
paroksizmleri izlenmektedir.
Epileptiform
anomaliler, diken
(70 ms’nin altında tabanı olan) ve keskin
(70-200 ms tabanlı) dalgalardır ve bu dalga formlarının
altında yatan fizyolojik olay paroksismal depolarizasyon kaymasıdır (Şekil 10). Yavaş
dalga ve epileptiform anomali
birlikte bulunabilir. Ancak tipik epileptiform
EEG anomalilerinin normal kişilerde de (normal
çocuklarda % 1,5-5 oranında) görülebildiği bilinmektedir. Tam tersine, epileptik
bir hastanın EEG incelemesinde sadece yavaş dalgalar görülebilir, hatta inceleme
tekrarları tamamen normal olabilir. Bu açıdan EEG değerlendiren hekim, klinisyeni bir tanıya yönlendirmekten kaçınmalıdır.

Şekil 10. Juvenil miyoklonik epilepsi tanısı olan bir olguda jeneralize
düzensiz diken-dalga deşarjlarından oluşan epileptiform
aktivite izlenmektedir.
Diğer EEG Teknikleri
Rutin EEG çekimi
dışında sık olarak uyku EEG’si (özellikle çocuklarda uyanıklık kaydı
güç elde edildiğinden), uzun süreli EEG, uyku deprivasyonlu
EEG gibi, epilepsi odağını tetiklemeyi amaçlayan, temelde aynı ama bazı süre
ve durum farklılıkları olan incelemeler planlanabilir. EEG “mapping” denen yöntem EEG dalgalarının frekanslarının
haritalanması ilkesine dayanır ve görsel analize üstünlüğü olmadığı gösterildiğinden
kullanılmamaktadır.
Dijital EEG’lerin
kullanımının artması ile geliştirilen devamlı video EEG monitorizasyon incelemesinde hastanın görüntüsü
ve EEG eş zamanlı olarak kaydedilmekte ve bulgular çok daha detaylı bir şekilde
karşılaştırmalı olarak incelenebilmektedir. Bu yöntem başlıca epilepsiyi
taklit eden durumlardan ayırmak, nöbet tipini kesin olarak belirlemek ve
nöbete eşlik eden semiyolojik özellikleri gözlemlemek
için kullanılır. En önemli ve sık kullanım nedenlerinden biri de, ilaç tedavisine
dirençli olgularda nöbet kaydı yapılarak sorumlu epileptojenik
odağın belirlenmesi ve epilepsi cerrahisine hazırlıktır. Video-EEG monitorizasyon bu anlamda epilepsi cerrahisinin olmazsa
olmazıdır. Noninvazif yani yüzeyel video-EEG
ile odak gösterilemediğinde ayrıntılı klinik ve görüntüleme analizlerinin
de yardımıyla o hasta için bir yaklaşım belirlenip invazif EEG de yapılabilmektedir.
İnvazif video-EEG’de hastadaki epilepsi odağının durumuna ve yerleşimine
göre beyin parenkimine stereotaktik
derin elektrodların veya subdural “grid” ve “strip” denen elektrodların
yerleştirilmesi söz konusudur. Bu teknikler, infeksiyon ve kanama başta olmak
üzere riskler taşımaları açısından noninvazif
EEG’den farklılık gösterirler. Semi-invazif deyimi ise foramen ovale düzeyinde yerleştirilen elektrodları içerir. Çok ağrılı olması ve fazla bir
üstünlüğü olmaması nedeniyle seyrek olarak uygulanır.
Video-EEG’nin
yorumlanması ciddi bir iktal EEG ve klinik nöbet
semiyolojisi bilgisi gerektirir, bu nedenle epilepsi merkezlerinde yapılması
daha uygundur. Video-EEG’nin klinik pratikte önemli bilgiler verdiği bir
konu da psikojen non-epileptik nöbetlerin ya
da diğer adıyla psödo-nöbetlerin tanınmasıdır.
Psödo-nöbetli bir hastanın boş yere yanlış bir
tanıyla gereksiz antiepileptik ilaç almasının önüne geçilmiş ve gereken doğru
tedavinin planlanmasına olanak sağlanmış olur. Tam tersine psödonöbet sanılan bir tablonun aslında gerçekte epilepsi
nöbeti olduğu görülebilir. Bu durum özellikle frontal lob kökenli nöbetlerde
söz konusudur.
Başlangıçta sadece
epilepsi merkezlerinde kullanılan video-EEG monitorizasyon
incelemesi modern bilgisayar teknolojisinin gelişmesi ile son yıllarda yoğun
bakım ünitelerinde de daha yaygın kullanılır hale gelmiştir. Özel bir program
ile parametrelerin spektral analizi yapılabilir hale gelmiş, bu analizler
histogramlar ile görüntülenebilir olmuştur. Ayrıca
serebral perfüzyon basıncı (SPB), kafa içi basınç (KİB) ve parsiyel oksijen
basıncı (pO2) gibi bir çok fizyolojik parametreyle
birlikte eş zamanlı olarak EEG monitorizasyonu
yapılabilmektedir. Bu şekilde çok sayıda modalitenin
birlikte izlenmesi fizyolojik değişkenlerin kontrolümüzde olmasını sağlar.
Ancak farklı fizyolojik modalitelerle kombine
edilerek multimodal monitorizasyon
olanağı sağlasa da deneyimli bir göz tarafından görsel analizin yapılmadığı,
sadece kantitatif EEG monitorizasyonun
yapıldığı durumlarda artefaktlara karşı çok dikkatli
olunması gerektiği de unutulmamalıdır. Yoğun bakım ünitesinde devamlı
EEG monitorizasyonu (dEEGm)
sistemik veya nörolojik nedenlere bağlı gelişen koma tablosundaki hastaların
takibinde giderek daha fazla kullanılmaktadır. Özellikle nonkonvülzif nöbetler ve iskemi
için yüksek riskli hastalarda multimodal monitorizasyonun ayrılmaz bir parçasını oluşturur.
Ayrıca farmakolojik komada doz titrasyonu ve
komada prognoz tayininde de kullanılır.
Polisomnografi
Uyku
hastalıklarının çoğunun tanısında altın standart olarak kabul edilen polisomnografi (PSG) tetkiki farklı fizyolojik sinyallerin
kaydedilmesinden oluşur. Polisomnografi kelimesi
Eski Yunanca’da birçok
anlamına gelen polus (πολύς), Latince’de uyku anlamına gelen somnus ve yine Eski Yunanca’da
yazmak, yazdırmak anlamına gele graphein (γράφειν) kelimelerinden köken almaktadır. Genel olarak
kaydedilen veriler video, EEG, elektrookülografi
(EOG), çene ve tibialis anterior
kaslarının yüzeyel EMG’si, hava akımı sinyalleri, solunum eforu sinyalleri, oksijen satürasyonu,
vücut pozisyonu ve elektrokardiyografidir (EKG). Hastaların ön tanısına göre
genişletilmiş EEG derivasyonları, ek EMG elektrotları, karbondioksit satürasyon ölçerleri, kan basıncı monitörleri ve özefageal pHmetreler gibi
parametreler eklenebilir veya ideal tedavinin belirlenmesi için pozitif hava
yolu basıncı sağlayan cihazlarla titrasyon işlemi
gerçekleştirilebilir. Bu konuda eğitim almış teknisyenler tarafından gece
boyunca gözetim altında gerçekleştirilen kayıt, somnologlar
(uyku uzmanları) tarafından değerlendirilir. Gün içi aşırı uykululukla seyreden
tabloların tanısında kullanılan gündüz çoklu uyku latans testleri ve uyanıklığın
sürdürülmesi testleri de PSG kayıtlama ile gerçekleştirilen testlerdir.
Polisomnografi
ile toplam uyku süresi, uyku etkinliği, uyku ve REM latansı, uyku evrelerinin
süresi, uyanıklık reaksiyonları, uykudaki kardiyak ritim anomalileri, periyodik bacak hareketleri gibi kas aktiviteleri,
apne ve hipopneler
gibi solunum olayları, hipoventilasyon varlığı,
periyodik solunum gibi özel solunum paternleri,
parasomniler ve EEG anomalileri saptanabilir.
(Ayrıca bakınız: Uyku Bozuklukları).
Polisomnografi
temel olarak uyku ilişkili solunum bozuklukları, hipersomniler,
uyku ilişkili hareket bozuklukları, parasomniler
ve seçilmiş insomni hastalarının tanısında kullanılır.
Bunun yanı sıra noktürnal nöbetlerin ayırıcı
tanısı için de çok faydalı bir yol göstericidir. Günümüzde en önemli endikasyonu olan ve ciddi bir toplum sağlığı problemi
teşkil eden uyku apnesinin tanısının konulması
ve tedavisinin planlanmasında PSG altın standarttır. Ancak komplike olmayan hastalarda, ayırıcı tanıda farklı
uyku hastalıkları düşünülmüyorsa, daha kısıtlı parametrelerle kayıt yapan
telemetrik uyku apne
testi cihazları da kullanılabilir.
Çoğu
insomni tablosunun ve sirkadyen
ritim bozukluklarının değerlendirilmesinde PSG endikasyonu
yoktur. Sirkadyen ritim bozukluklarının değerlendirilmesinde
seçilecek tetkik uyku günlükleri ve aktigrafi
olmalıdır. Aktigraflar kol saatine benzer küçük
cihazlardır ve takıldıkları sürece kişinin dinlenme/aktivite sikluslarını kaydeder, bu veriyi analiz ederek tahmini
bir uyku profili çıkarırlar (Şekil
11). Ön tanıya göre 1-2 hafta süreyle takılırlar, bu sayede kişinin hem
iş günlerindeki, hem de tatil günlerindeki uyku alışkanlıkları hakkında bilgi
vermeleri sağlanır. Tercihen beraberinde tutulan bir uyku günlüğü ile birlikte
yorumlanırlar. Bazı cihazlarda bulunan ışık sensörü,
kişinin maruz kaldığı ışık miktarının ve maruz kalınan ışığın dalga boyunun
da saptanmasını mümkün kılar. Hem kullanım kolaylığı, hem uzun süreli kayıt
imkanı, hem de ucuz maliyeti açısından geniş ölçekli
araştırmalar için uygun olsalar da, aktigraflar
ancak kısıtlı veri sağlayabildikleri için PSG’nin
yerini tutabilecek cihazlar değildir. Dolayısıyla yukarıda belirtilen az
sayıda endikasyon dışında rutin tanı ve tedavi
süreçlerinde kullanılmamaktadırlar.

Şekil 11. Normal
bir aktigrafi kaydı örneği. Her bir satır 24
saati temsil etmektedir. Uyku epizodları gri
renk ile işaretlenmiştir. Grafikteki siyah çizgiler bireyin hareketlerini,
gri çizgiler ise farklı frekanslardaki ışık maruziyetini
temsil etmektedir.
EEG’nin Klinikteki
Kullanımı
Epilepsili hastalarda
karakteristik epileptiform EEG bulguları ile
klinik tanı doğrulanabilir. EEG bulgularına göre nöbet tipi ve epilepsi sendromu gruplanabilir. Ancak, normal bir EEG’nin epilepsi
tanısını dışlamaya yetmeyeceği unutulmamalıdır. İlk rutin EEG ile epilepsili
olguların ancak %30-50’sinde tipik patolojik bulgu görülürken, 3. EEG ve
provokasyon yöntemleri ile patolojik bulgu oranı
%60-90’a yükselir. Çok önemli bir nokta da deneyimli EEG okuyucularının bile
aralarındaki uyumun ancak %70’lerde olması yani EEG’nin yorumlanmasının ciddi
sübjektivite gösterebilmesidir. Bu nedenle klinik açıdan kritik kararlar
alınırken EEG’lerin klinik nörofizyologlara danışılması
önerilmelidir.
İlk epilepsi
nöbetini geçirmiş olan bir hastada tedaviye başlama kararı sırasında veya
remisyona girdiği düşünülerek tedavinin sonlandırılması
planlanan olgularda EEG tek başına karar verdirmese de çok yararlı bilgiler
sağlar. EEG’de patolojik bulgular olması nöbet tekrarı açısından önemli risk
faktörüdür, ancak tek belirleyici olarak algılanmamalıdır.
Rutin
bir EEG’de de zaman zaman nöbet kayıtları yapılabilmektedir. Bu nedenle iktal EEG paternlerinin
ayrıntılı şekilde bilinmesi önemlidir. Nadir olan bir durum da hastada klinik
olarak bir nöbet söz konusu değilken elektrofizyolojik nöbet kaydı olabilmesidir.
Status epileptikusda EEG takibi çok önem taşır,
status epileptikus için farklı nöbet paternleri olduğu bilinmektedir (Şekil 12).
Nonkonvülzif status epileptikus
tanısı için ise EEG vazgeçilmez ve kesin tanı koyduran yöntemdir (Şekil
13).
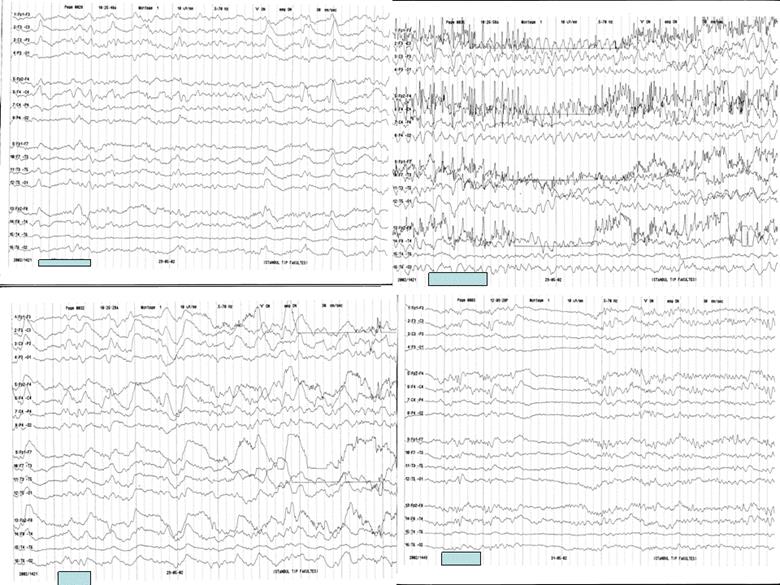
Şekil 12. Status
epileptikus tablosu günlerce süren bir olguda
farklı zamanlarda EEG bulgularının değişkenliği izlenmektedir.
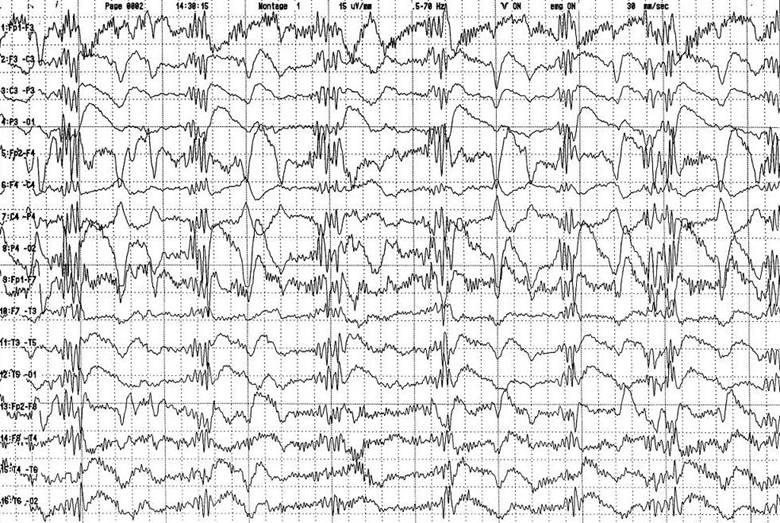
Şekil 13.
Garip davranışlar ve uyku hali nedeniyle getirilen hastanın EEG’sinde non-konvülzif status epileptikus
ön tanısını destekleyen elektrofizyolojik bulgular izlenmektedir.
Epilepsi bölümünde
çeşitli epileptik sendromların spesifik EEG bulguları
üzerinde durulmuştur bu nedenle bu bölümün incelenmesi önerilir (Bakınız:
Epilepsi).
Epilepsili olguların nöbet geçirmemiş aile bireyleri incelendiğinde tipik
epileptiform bulgulara rastlanabilmektedir.
EEG’nin ana kullanım
alanı epilepsi hastalarını değerlendirmek olmakla birlikte, çok önemli ve
vazgeçilmez olduğu diğer bir kullanım alanı uyanıklık kusuru ve komada olan
hastalarda ayırıcı tanı, tedavinin izlenmesi ve prognoz tayinidir. Bu hastaların
EEG incelemelerinde saptanan bazı aktiviteler bize komanın derinliği hakkında
da bilgi verir. Hafif bilinç bozukluklarında alfa aktivitesinde azalma, teta-delta aktivitesinde artma izlenirken, koma tablosu
ağırlaştıkça daha karakteristik paternler izlenir.
Bu dönemdeki hızlı aktiviteler daha çok benzodiazepin
veya barbitürat gibi ilaç kullanımına bağlıdır.
İzleyen bölümde
bazı önemli EEG paternleri üzerinde kısaca durulacaktır:
Aralıklı ritmik
delta aktivitesi (RDA); 2-3 Hz sinüzoidal delta aktivitesi ile karakterize,
ritmik ve aralıklı ortaya çıkan, daha çok komanın erken dönemlerinde izlenen
aktivitelerdir. Erişkinde çoğunlukla frontal bölgelerde belirirken (FIRDA),
çocuklarda genellikle hemisfer arka yarıları
üzerinde görülür. Çoğunlukla simetrik ve senkron bir şekilde ortaya çıkan
bu aktivite göz açma ile kaybolur. Nonspesifik bir bulgu olup metabolik-toksik
ensefalopatilerde, talamo-kortikal
bağlantıları kesintiye uğratan orta hat lezyonlarında, III. ventrikülde basınç artışında ve kortiko-subkortikal yapıları yaygın olarak etkileyen
klinik tablolarda saptanabilir. Prognoz da altta yatan etyolojiye bağlıdır. Oksipital aralıklı ritmik delta
aktivitesi (OIRDA) ise absans nöbetleri olan
jeneralize epilepsilerde görülebilir, ancak iktal bir patern değildir.
Temporal yerleşimi olan benzer dalgalar yani TIRDA temporal lob epilepsisinde
sıkça görülür.
Uzamış yavaş
dalga aktivitesi; farklı etyolojilere
bağlı gelişen derin koma tablolarında görülebilir. Çoğunlukla her iki hemisfer üzerinde yaygın bir şekilde belirir, bazen
lateralize de olabilir fakat evolüsyon görülmez.
Dış uyaranlara reaktif olan 1 Hz’den büyük delta
aktivilerinde prognoz görece daha iyidir.
Burst-supresyon (boşalım-baskılanım) paterni; günümüzde sadece derin koma tabloları
ve bazı nadir çocukluk çağı ensefalopatilerinde
(Ohtahara sendromu) bildirilirken, bu patern orijinal tanımlanmasında derin anestezi sırasındaki
EEG bulgusu olarak rapor edilmiştir. Ancak bugün anoksik
koma tablolarında kötü prognoz kriteri olduğu bilinmektedir. Bunun dışında
farklı etyolojilere bağlı (yapısal, toksik ve
metabolik) koma tablolarında veya hipotermi sırasında
saptanabilir. Genellikle 1-10 saniye süren, periyodik, yüksek amplitüdlü,
veya salvolar halinde beliren keskin kontürlü,
diken, çoklu diken-dalga aktivitelerini takip eden supresyon
dönemleri ile karakterizedir. Supresyon periyodu
tam baskılanmış, izoelektrik hat şeklinde olabilir
veya düşük amplitüdlü ritimlerden oluşabilir. Hasta derin komada olabildiği
gibi bu sırada yüz, kol, göğüs ve bacaklarda miyoklonik
atmalar görülebilir. Çoğu hastada dış uyaran ile ortaya çıkabilir.
Alfa-teta koma paternleri ve
uyku benzeri aktiviteler; alfa-teta koma, anoksik komada olabildiği gibi beyinsapı iskemisi
veya tümörü gibi nedenlere bağlı koma tablolarında görülebilir. Uyanıklıkta
görülen alfa ritminin aksine komadaki alfa aktivitesi yaygındır, hemisfer ön yarılarında daha belirgindir, dış uyarana
reaktif değildir. Tipik spasyotemporal evolüsyon
görülmez ama bir iktal aktivite alfa koma paterni
zemininde gelişebilir. Uyku iğcikleri, yavaş
aktivite, K-kompleksleri ve uyanma reaksiyonu gibi uykunun fizyolojik aktivitelerine
benzer aktiviteler de koma tablolarında görülebilir. Fizyolojik uyku iğciklerine göre daha hızlı veya yavaş frekansta ve
daha uzun sürelerle görülebilirler.
Trifazik dalgalar (TD);
yüksek amplitüdlü pozitif keskin dalgayı takip eden düşük amplitüdlü negatif
dalgadan oluşan, 3 fazlı, künt 2-3 Hz çentikli
delta dalgalarıdır. Bazı tartışmalı yanları nedeniyle yeni terminolojide
devamlı, trifazik morfolojili,
2 Hz, jeneralize periyodik deşarjlar (PD) olarak tanımlanmıştır. TD öncelikle
metabolik koma nedenlerini, özellikle hepatik (Şekil 14) ve üremik
komaları akla getirse de farklı etyolojilere
bağlı koma tablolarında da görülebilir. Hatta trifazik
morfolojili jeneralize
keskin dalgalar ağır bir epileptik ensefalopati
olan Lennox-Gastaut sendromunda
bile görülebilirler.

Şekil 14. Bir hepatik ensefalopati olgusunda tipik trifazik dalgalar görülmektedir.
Ritmik periyodik
paternler ise hastaların dEEGm ile izlenmeleri yaygınlaştıkça daha fazla rastlanmaya
başlamış ve bu paternler 2013 yılında yayınlanan
son kılavuza göre RDA, PD, ritmik diken ya da keskin dalga aktivitesi (RDD)
olarak üç başlıkta gruplandırılmışlardır. Buna göre PD ardışık dalga formları
arasında ölçülebilir ve tanımlanabilir bir deşarj aralığının olduğu, aynı
morfoloji ve sürede tekrarlayan, düzenli aralıklarla ortaya çıkan dalga formudur
(Şekil 15a). Bir paternin periyodik ve
ritmik olabilmesi için en az 6 döngü boyunca devam etmesi gerekmektedir (6
saniye boyunca 1/saniye veya 2 saniye boyunca 3/saniye gibi). RDA ise ardışık
dalga formları arasında ölçülebilir ve tanımlanabilir bir deşarj aralığının
olmadığı aynı morfoloji ve sürede tekrarlayan delta frekansındaki dalga formudur
(Şekil 15b). RDD de diken/keskin dalga aktivitesini çoğunlukla bir
yavaş dalganın izlediği, ardışık dalga formları arasında ölçülebilir ve tanımlanabilir
bir deşarj aralığının olmadığı aynı morfoloji ve sürede tekrarlayan aktivitelerdir
(Şekil 15c). Bütün bu ritmik periyodik paternler
lokalizasyonlarına göre jeneralize, lateralize, bilateral birbirinden bağımsız lateralize ve multifokal olarak tanımlanırlar. Jeneralize PD talamokortikal
yolların, kortikal inhibitör nöronların etkilendiği
metabolik, yapısal koma tablolarında da görülebilir (Şekil 16). Bu
aktivitelerin bazen iktal olarak değerlendirilmesi
ve tedavi gerekliliği konusunda araştırmalar sürmektedir; frekans, lokalizasyon
ve morfolojide net evolüsyon gösteriyorsa veya yüzde atma, göz deviyasyonu gibi sinsi motor semptomlara eşlik eden
30 dakikadan uzun süren jeneralize PD var ise iktal
olarak tanımlanmıştır. Lateralize PD ya da eskiden
kullanılan ve daha iyi bilinen adıyla PLED klinik
ve MRG bulgularıyla bir araya getirilerek Herpes simpleks
ensefaliti gibi çok hızla tanı konup tedavi edilmesi gereken tablolarda tanıya
varmada değer taşır (Şekil 17). Ayrıca PLED bulgusu akut inme gibi
akut ve haraplayıcı bir beyin lezyonunu da yansıtabilir
ve nöbetlerle önemli oranda ilişkilidir (Şekil 18).

Şekil 15a-b-c. Alfabetik sıraya
göre alt alta Amerikan Klinik Nörofizyoloji Derneği’nin
son yayınlanan kılavuzuna göre tanımlanan periyodik deşarj, ritmik delta
aktivitesi ve ritmik diken ya da keskin dalga aktivitesi örnekleri izlenmektedir.

Şekil 16. Ağır hepatik yetmezlikteki
bir hastada izlenen jeneralize periyodik deşarjlar görülmektedir.

Şekil 17. Sol hemisfer üzerinde periyodik lateralize
epilpetiform deşarj (PLED) izlenen bu hasta Herpes
simpleks ensefaliti tanısı almıştır. Hastanın
sağ hemisferinde de yavaş dalgaların olduğu görülmektedir
(Tek sayılı elektrodlar sol, çift sayılı olanlar
ise sağ hemisferin ilgili bölgelerine işaret
etmektedir).
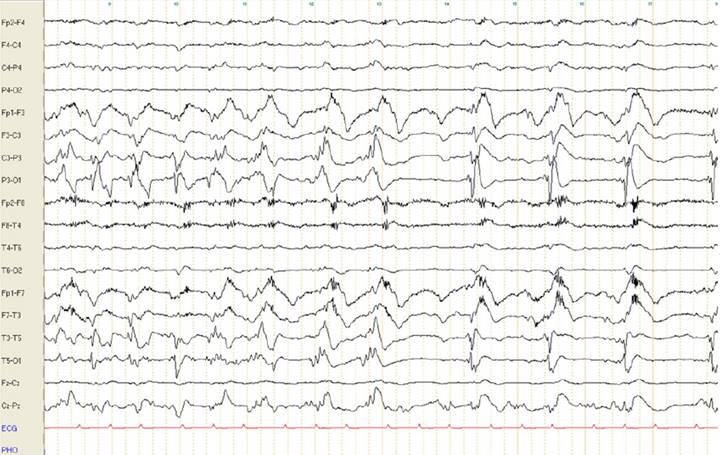
Şekil 18. Sağ hemiplejik kadın hastanın EEG incelemesinde eski terminoloji
ile PLED aktivitesi izlenmektedir.
Kısa potansiyel
iktal ritmik deşarj olarak tanımlanan BIRDs adlı aktivite ise primer beyin hasarı olan,
komadaki hasta grubunda saptanmıştır. “Stimulus-induced”
ritmik periyodik patern (SIRPID); komadaki
hastalarda, herhangi bir uyaran ile ortaya çıkan ve uyaran süresince devam
eden iktal görünümlü veya periyodik dalgalardır.
NKSE
tanısında EEG bulgularının yorumlanması bazı durumlarda soru işaretleri yaratmaktadır.
Bu nedenle düzenlenen uluslar arası toplantılar
sonrasında “Salzburg Konsensus Ölçütleri” geliştirilmiştir.
Bu ölçütlerin Amerikan Klinik Nörofizyoloji Topluluğu
2012 kriterlerine göre modifiye edilerek uygulandığı
50 ardışık non-hipoksik NKSE olgusunda yapılan retrospektif
bir çalışmada tanı açısından başarılı sonuçlar elde edilmiştir. Salzburg
kriterleri aşağıdaki tabloda özetlenmiştir.
Tablo
1.
Non-konvülzif status epileptikus
için Salzburg Konsensus Kriterleri
|
A.
Epileptik ensefalopatisi olmayan bir hastada
10 saniyeden uzun süren, 1.
>2,5 Hz ED 2.
ED ≤2,5 Hz veya ritmik delta/teta aktivite >0,5
Hz ise aşağıdakilerden
en az 1’i eşlik ediyorsa iktal olarak tanımlanmıştır. En
az biri eşlik etmesi gereken diğer bulgular: a)
Damar
içi AEİ uygulaması
ile klinik ve EEG’de
düzelme, b)
Eşlik
eden sinsi
klinik bulgu
varlığı, c)
Tipik
spasyotemporal evolüsyon*.
Klinik
düzelme olmaksızın EEG’de düzelme olması veya evolüsyon olmaksızın dalgalanma**
olması durumunda klinik tablo olası NKSE olarak tanımlanır. |
|
B.
Bilinen epileptik ensefalopatisi olan bir hastada
A’daki kriterlere ek olarak aşağıdaki kriterlerden
birinin olması gerekir. Bu kriterler: 1.
Klinik
durumdaki belirgin
değişikliğe eşlik
eden EEG’de
ED’de görünüm
ve sıklıkta belirgin
artış, 2.
Damar
içi AEİ kullanımı
ile klinik ve EEG’de
düzelme. |
|
ED:
Epileptiform deşarj, AEİ: Antiepileptik
ilaç, EEG: Elektroensefalografi, NKSE: Non-konvülzif status epileptikus.
|
|
*Spasyotemporal evolüsyon, frekans (en az 0,5 Hz),
morfoloji (en az 2 morfolojik değişiklik) ve lokalizasyon (en az 2 elektrod) kriterlerinin
en az ikisinde ardışık, en az 3 siklus süren,
çok belirgin değişikliktir. **Dalgalanma
ise 1 dakikadan uzun sürmeyen, frekans (en az 0,5 Hz), morfoloji (alterne eden en az 2 morfolojik özelliğin en az
3 kez değişiklik göstermesi), lokalizasyonda (en az 1 elektrod veya diğerleri), en az 3 kez izlenen değişikliktir. |
Kaynaklar
1.
Aykut-Bingöl
C, Çelik M, Gürtekin
Y: Klinik Nörofizyoloji
Laboratuvarları Uygulama
El kitabı.1.Baskı. Namaş
AŞ, İstanbul, 2006.
2.
Baykan
B, Altındağ E. Nonkonvülzif
Status Epileptikus. Cortex Yayıncılık İstanbul, 2018.
3.
Bora İ, Yeni SN: EEG Atlası. Nobel
Tıp Kitabevi, İstanbul, 2012.
4.
Kane N, Acharya
J, Benizcky S, Caboclo
S, Finnigan S, Kaplan PW, Shibasaki H, Pressler R,
van Putten M. A Revised Glossary of Terms Most
Commonly Used by Clinical Electroencepaholgraphers and Updated Proposal
for the Report Format of the EEG Findings. Revision 2017. Clinical Neurophysiology
Practice. 2017;2;170-85.
5.
Velis
D, Plouin P, Gotman
J, Lopes da Silva F.( members of the ILAE DMC
Subcommittee on Neurophysiology). Recommendations Regarding the Requirements
and Applications for Long-term Recordings in Epilepsy. Epilepsia. 2007;48:379-84.
6.
Hirsch
LJ, Laroche SM, Gaspard
N, Gerard E, Svoronos
A, Herman ST, Mani R, Arif H, Jette N, Minazad Y, Kerrigan JF,
Vespa P, Hantus S,
Claassen J, Young
GB, So E, Kaplan PW, Nuwer
MR, Fountain NB, Drislane
FW. American Clinical
Neurophysiology Society’s
Standardized Critical Care
EEG Terminology: 2012 version.
J Clin Neurophysiol
2013; 30:1-27.
7.
Leitinger
M, Beniczky S, Rohracher
A, Gardella E, Kalss
G, Qerama E, Höfler
J, Hess Lindberg-Larsen
A, Kuchukhidze G, Dobesberger
J, Langthaler PB, Trinka
E. Salzburg Consensus Criteria
for Non-Convulsive
Status Epilepticus: Approach
to clinical application. Epilepsy
Behav. 2015;49:158-63.
8.
Leitinger
M, Trinka E , Gardella E , et al. Diagnostic
accuracy of the Salzburg
EEG criteria for
non‐convulsive status epilepticus:
a retrospective study
. Lancet Neurology.
2016 ;15:1054 – 62
9.
Bassetti
CL, Đogaš Z, Peigneux
P, ESRS European Sleep Medicine Textbook, European Sleep Research Society
(ESRS), Regensburg, 2014